�߿����W��݆�������ن��|�X֪�R�c���}���Y
2019-01-07 17:15:26���þW
����1���X��ԭ�ӽY��
�����Xλ��Ԫ�����ڱ��е������ڢ�A�壬�������3����ӣ��ڻ��W��������ʧȥ��Ӷ����F�飫3�r���X�ڵؚ��к����S�����H����������Ȼ���е��Xȫ���Ի��ϑB��ʽ���ڡ�
������ע��
�����ٳ����£������X������ʢ�ŝ����ᡢ�������ԭ���Ƕ�����ʹ�X�l��“�g��”���������X�c�����ᡢ�����������
�������X�cϡ���ᷴ���r���ɵĚ��w��NO������H2��
���������c�X�����a��������Һ���ܳʏ�����Ҳ���ܳʏ��A�ԡ�

����(2)��;
�����ټ��X����������
�������X�Ͻ��Ƃ���܇���w�C��������Ʒ�ȡ�
�����X����Ҫ������——�����X���������X
����1�������X
����(1)�������|����ɫ���w���y����ˮ���кܸߵ����c��
����(2)���W���|�����ڃ��������

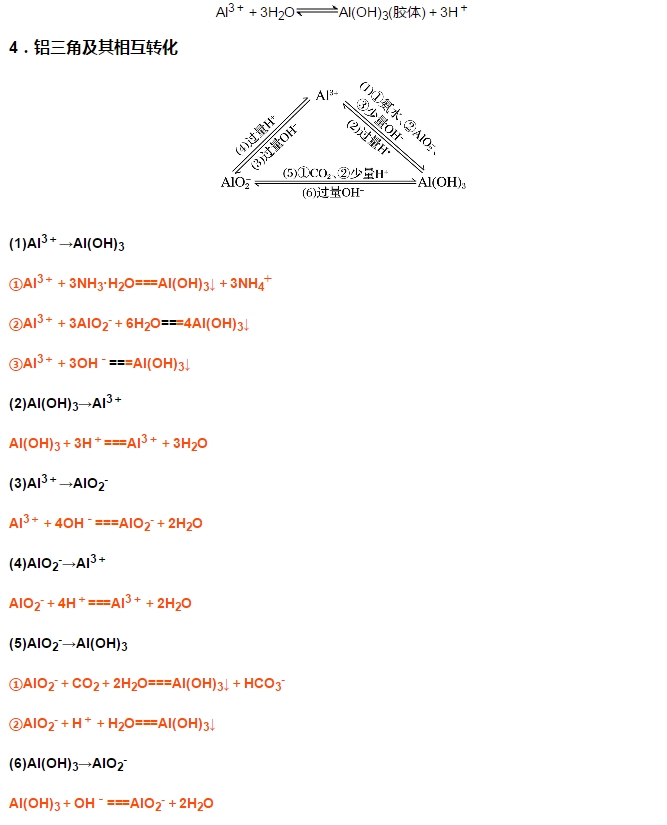

�����c�X���P�ĈD�����
����1.��������X�}��Һ����μ���NaOH��Һ���^��

















